
L’Associazione conSLAncio Onlus, fondata da Andrea Zicchieri, aderente all’International Alliance of ALS/MND Associations (Alleanza Internazionale delle Associazioni SLA/MND) e EUpALS (Organizzazione Europea per professionisti e pazienti affetti da SLA), era presente al 34° Simposio Internazionale sulla SLA/MND, 6-8 Dicembre 2023 a Basilea, Svizzera. Questo Simposio è la più grande conferenza al mondo sulla Sclerosi Laterale Amiotrofica (SLA) organizzata dalla Motor Neurone Disease Association. L’edizione 2023 ha ospitato oltre 1.300 delegati in persona e 350 delegati online, da 44 nazioni, incluso medici, ricercatori, pazienti, caregiver ed organizzazioni della comunità SLA internazionale.
.
conSLAncio vi presenta il più completo resoconto del simposio in Italiano.
 Durante l’inaugurazione del congresso, l’International Alliance of ALS/MND Associations ha conferito il Premio Forbes Norris Award 2023 al Prof. Jeremy M. Shefner, M.D., PhD, medico e direttore della Neurologia presso il Barrow Neurological Institute di Phoenix, Arizona, Stati Uniti. Questo premio rappresenta il massimo riconoscimento globale nel campo clinico sulla SLA e premia l’attenzione alla cura e all’assistenza dei pazienti ed il progresso delle conoscenze scientifiche. Prima al Brigham and Women’s Hospital alla SUNY Upstate Medical University e ora al Barrow Neurological Institute, il prof. Shefner ha diagnosticato e curato innumerevoli pazienti affetti da SLA negli Stati Uniti. Il suo approccio alla cura dei pazienti è olistico e integra trattamento medico, supporto psicosociale e partecipazione attiva alla ricerca clinica. Il suo sostegno alla ricerca e alle iniziative di miglioramento della qualità della ricerca stessa ha fatto progredire in modo significativo l’assistenza multidisciplinare ai pazienti affetti da SLA. I pazienti ne apprezzano universalmente l’empatia, la sicurezza e il comportamento compassionevole. Il suo impegno a dedicare molto tempo alla clinica e a garantire che le esigenze dei pazienti siano soddisfatte riflette la sua genuina dedizione al miglioramento della qualità di vita delle persone affette da SLA. Nel campo della ricerca sulla SLA, l’impatto del prof. Shefner è fondamentale. Il suo ruolo di principal investigator in numerosi studi clinici di fase 2 e 3 ha un contributo fondamentale allo sviluppo di risultati che hanno ampliato le opportunità di sperimentazione clinica per i pazienti affetti da SLA. Cofondatore del Northeast ALS Consortium (NEALS), il prof. Shefner ha trasformato la ricerca clinica sulla SLA a livello mondiale, fornendo infrastrutture e competenze che hanno portato ad un aumento delle opportunità di sperimentazione. Molte terapie promettenti devono il loro sviluppo al Consorzio NEALS.
Durante l’inaugurazione del congresso, l’International Alliance of ALS/MND Associations ha conferito il Premio Forbes Norris Award 2023 al Prof. Jeremy M. Shefner, M.D., PhD, medico e direttore della Neurologia presso il Barrow Neurological Institute di Phoenix, Arizona, Stati Uniti. Questo premio rappresenta il massimo riconoscimento globale nel campo clinico sulla SLA e premia l’attenzione alla cura e all’assistenza dei pazienti ed il progresso delle conoscenze scientifiche. Prima al Brigham and Women’s Hospital alla SUNY Upstate Medical University e ora al Barrow Neurological Institute, il prof. Shefner ha diagnosticato e curato innumerevoli pazienti affetti da SLA negli Stati Uniti. Il suo approccio alla cura dei pazienti è olistico e integra trattamento medico, supporto psicosociale e partecipazione attiva alla ricerca clinica. Il suo sostegno alla ricerca e alle iniziative di miglioramento della qualità della ricerca stessa ha fatto progredire in modo significativo l’assistenza multidisciplinare ai pazienti affetti da SLA. I pazienti ne apprezzano universalmente l’empatia, la sicurezza e il comportamento compassionevole. Il suo impegno a dedicare molto tempo alla clinica e a garantire che le esigenze dei pazienti siano soddisfatte riflette la sua genuina dedizione al miglioramento della qualità di vita delle persone affette da SLA. Nel campo della ricerca sulla SLA, l’impatto del prof. Shefner è fondamentale. Il suo ruolo di principal investigator in numerosi studi clinici di fase 2 e 3 ha un contributo fondamentale allo sviluppo di risultati che hanno ampliato le opportunità di sperimentazione clinica per i pazienti affetti da SLA. Cofondatore del Northeast ALS Consortium (NEALS), il prof. Shefner ha trasformato la ricerca clinica sulla SLA a livello mondiale, fornendo infrastrutture e competenze che hanno portato ad un aumento delle opportunità di sperimentazione. Molte terapie promettenti devono il loro sviluppo al Consorzio NEALS.
<<>>
.
 La Dott.ssa Alyssa Coyne, PhD, della John Hopkins University School of Medicine ha vinto il 15° Premio Paulo Gontijo Award 2023. Il Premio Paulo Gontijo, noto anche come PG Award, premia dal 2007 giovani ricercatori di tutto il mondo impegnati nella ricerca delle cause e delle cure della SLA. Si tratta di un premio in onore di Paulo Gontijo, forte sostenitore della ricerca cui è dedicato anche l’Istituto Paulo Gontijo.
La Dott.ssa Alyssa Coyne, PhD, della John Hopkins University School of Medicine ha vinto il 15° Premio Paulo Gontijo Award 2023. Il Premio Paulo Gontijo, noto anche come PG Award, premia dal 2007 giovani ricercatori di tutto il mondo impegnati nella ricerca delle cause e delle cure della SLA. Si tratta di un premio in onore di Paulo Gontijo, forte sostenitore della ricerca cui è dedicato anche l’Istituto Paulo Gontijo.
La Dott.ssa Coyne è professore associato presso il Dipartimento di Neurologia, Brain Science Institute della Johns Hopkins University School of Medicine (USA), e ha presentato la tesi, “Therapeutically targeting NPC injury cascades to alleviate TDP-43 dysfunction in ALS”. Come riconoscimento ha ricevuto una medaglia d’oro e un finanziamento scientifico di 10.000 dollari.
<<>>
.
 La Dott.ssa Lucie Bruijn, PhD ha vinto il Premio Humanitarian Award 2023 dall’International Alliance of ALS/MND Associations. Questo prestigioso riconoscimento onora la dedizione della Dott.ssa Bruijn nel migliorare la qualità della vita delle persone affette da SLA in tutto il mondo. Con una carriera illustre che abbraccia tre decenni, tra cui quella di vicepresidente senior per la ricerca e lo sviluppo e capo dell’ALS Association statunitense, la dott.ssa Bruijn ha svolto un ruolo fondamentale nel promuovere la ricerca sulla SLA a livello mondiale. Il suo lavoro pionieristico comprende la creazione del Programma di Ricerca dell’ALS Association e l’innovativa iniziativa TREAT ALS, che ha stabilito nuovi standard per la ricerca traslazionale sulla SLA.
La Dott.ssa Lucie Bruijn, PhD ha vinto il Premio Humanitarian Award 2023 dall’International Alliance of ALS/MND Associations. Questo prestigioso riconoscimento onora la dedizione della Dott.ssa Bruijn nel migliorare la qualità della vita delle persone affette da SLA in tutto il mondo. Con una carriera illustre che abbraccia tre decenni, tra cui quella di vicepresidente senior per la ricerca e lo sviluppo e capo dell’ALS Association statunitense, la dott.ssa Bruijn ha svolto un ruolo fondamentale nel promuovere la ricerca sulla SLA a livello mondiale. Il suo lavoro pionieristico comprende la creazione del Programma di Ricerca dell’ALS Association e l’innovativa iniziativa TREAT ALS, che ha stabilito nuovi standard per la ricerca traslazionale sulla SLA.
L’impatto della dott.ssa Bruijn comprende anche il sostegno iniziale allo studio Pre-fALS, uno studio longitudinale di individui potenzialmente a rischio di sviluppare la SLA familiare, che ha aperto la strada allo studio ATLAS. Al di là dei risultati scientifici, l’approccio globale della dott.ssa Bruijn è stato determinante nel promuovere la collaborazione multidisciplinare. La promozione di numerose iniziative hanno plasmato il panorama globale della SLA e hanno fatto leva sui fondi dei donatori per un maggiore impatto.
.
Il 34° Simposio Internazionale sulla SLA/MND celebra il 4° anno consecutivo in cui la nostra associazione ha presentato un poster al congresso.
Il poster presentato da conSLAncio
 Il poster intitolato, CMS-15: “Improving Online Caregiver Training for ALS Patients in Italy: a two-year update” (Migliorare La Formazione Caregiver Online per Pazienti SLA in Italia: un aggiornamento dopo due anni), è stato presentato dalla Dott.ssa Stella Gagliardi, PhD.
Il poster intitolato, CMS-15: “Improving Online Caregiver Training for ALS Patients in Italy: a two-year update” (Migliorare La Formazione Caregiver Online per Pazienti SLA in Italia: un aggiornamento dopo due anni), è stato presentato dalla Dott.ssa Stella Gagliardi, PhD.
Di seguito la lista completa degli autori: A.D. Zicchieri, N. De Rossi, A. Desiderato, S.F. Conte, S. Pozzi, P. Contessa, M. Consonni, J.C. Ayala, M. Peviani, T. Petrozziello, E. Grossini, S. Gagliardi, S. Rota, F. De Marchi.
Abstract
Razionale: L’accessibilità alla formazione può contribuire a rispondere alle esigenze di supporto da parte di coloro che sono impegnati nell’assistenza ai pazienti. Per questo motivo, la formazione online è uno strumento efficace per facilitare la partecipazione di persone che vivono in regioni diverse o che non possono partecipare di persona.
Obiettivi: Lo studio mira a determinare se il corso online per i caregiver che si occupano di soggetti affetti da SLA e per i pazienti fragili complessi abbia il potenziale per migliorare l’accesso alla formazione dei caregiver a due anni dalla pubblicazione da parte dell’associazione conSLAncio.
Metodi: Il corso è stato sviluppato a partire da un innovativo approccio interdisciplinare noto come Design-Build (progettazione-costruzione) integrando il feedback della comunità italiana della SLA (1). Il programma è stato il primo ed è l’unico corso di formazione gratuito per caregiver disponibile su richiesta 24 ore al giorno, 7 giorni alla settimana, per i pazienti affetti da SLA e da fragilità complessa in Italia (2). Copre 14 argomenti in un formato facile da usufruire. Al termine del corso è stato chiesto agli utenti di compilare un questionario.
Risultati: Più di 200 utenti si sono iscritti dal lancio nel Gennaio 2021. Abbiamo ricevuto un totale di 86 questionari da partecipanti di tutta Italia e residenti all’estero, tra cui Svizzera e Canada. Suddivisi tra caregiver (n=31), operatori socio-sanitari (n=24) e altro personale (n=31). La maggior parte degli utenti ha raccomandato il corso ad altri, tranne uno che lo ha trovato troppo avanzato. Non sono state riscontrate differenze significative nel grado di soddisfazione tra i tre gruppi di utenti. Gli argomenti più consigliati (>64%) sono stati: nutrizione artificiale, gastrostomia endoscopica percutanea e sondino nasogastrico, concetti anatomici, ventilazione artificiale e accessi venosi. Il meno interessante (<44%) è stato l’argomento sulla comunicazione efficace.
Discussione e conclusioni: Abbiamo ottenuto un’ampia partecipazione in tutta Italia e all’estero. I dati hanno mostrato un miglioramento del coinvolgimento nella cura della SLA. Abbiamo in programma di continuare a espandere il programma migliorandone i contenuti sulla base del feedback ricevuto dagli utenti. Scarica il poster di conSLAncio in fondo della pagina sotto ‘Risorse Correlate’.
Bibliografia:
1. Zicchieri, A.D., Conte, S.F., De Rossi, N. CMS-27: Using a Design-Build Approach to Improve International ALS Research News Access in Italy. Poster presented at the Motor Neurone Disease Association Virtual 31st International Symposium on ALS/MND, 9-11 December 2020.
2. Zicchieri A et al. CMS-09: Improving Online Caregiver Training for ALS and Complex Fragile Patients Using Design-Build in Italy. Virtual 32nd International Symposium on ALS/MND, 7-10 December 2021.
conSLAncio desidera rivolgere una standing ovation alla straordinaria dedizione di persone affette di SLA, famiglie, assistenti, volontari della comunità italiana e di tutto il mondo che ci aiutano nella nostra missione:
Barbara Balestra, Ilaria Barone, Richard Bedlack, Mattia Belloni, Alessandro Boaro, Francesco Boccalatte, Lara Brambilla, Valentina Cattero, Simone Cimino, Angelica D’Amore, Angelina Mira d’Ercole, Martina de Majo, Enrico Doria, Vittoria A. Farallo, Ilaria Ghiro, Nicolò Giordano, Vittoria Lombardi, Ester Luna, Ilaria Luna, Sean Mannion, Nicola Marinelli, Paola Mastracco, Deborah Metzel, Elisabetta Mezzalira, Ostap Nalysnyk, Peter Nalepa, Cristina Onesta, Alessandra Pecora, Nicoletta Pireddu, Aleh Plotnikau, Elisabetta Pupillo, Grazia Santoruvo, Daisy Sproviero, Giulia Supino, Luca Zampedri e Cinzia Zicchieri.
.
.
C’erano 120 presentazioni su piattaforma e oltre 400 poster dal vivo, presentando le ultime novità scientifiche della SLA/MND. Segnaliamo alcuni studi clinici e poster che hanno fornito un aggiornamento importante.
.
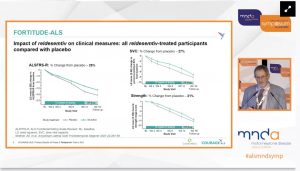 C60: Il prof. Jeremy Shefner, M.D., PhD del Barrows Neurological Institute (USA) ha presentato i risultati dello studio di fase 3 COURAGE-ALS sul Reldesemtiv dell’azienda Cytokinetics. Reldesemtiv è un attivatore selettivo della troponina muscolare scheletrica veloce (FSTA) che ha dimostrato di aumentare la forza di contrazione muscolare in risposta alla stimolazione nervosa in modelli animali e volontari sani. Uno studio precedente di fase 2 (FORTITUDE-ALS) aveva mostrato una forte tendenza all’efficacia nella variazione rispetto al basale per ALSFRS-R, SVC e forza. Sulla base dei risultati di FORTITUDE-ALS, COURAGE-ALS (NCT04944784) è stato progettato per testare l’efficacia di reldesemtiv in 555 partecipanti randomizzati (2:1) a ricevere reldesemtiv 300 mg BID o placebo, con un trattamento in doppio cieco per 24 settimane seguito da un periodo di 24 settimane di farmaco attivo in aperto.
C60: Il prof. Jeremy Shefner, M.D., PhD del Barrows Neurological Institute (USA) ha presentato i risultati dello studio di fase 3 COURAGE-ALS sul Reldesemtiv dell’azienda Cytokinetics. Reldesemtiv è un attivatore selettivo della troponina muscolare scheletrica veloce (FSTA) che ha dimostrato di aumentare la forza di contrazione muscolare in risposta alla stimolazione nervosa in modelli animali e volontari sani. Uno studio precedente di fase 2 (FORTITUDE-ALS) aveva mostrato una forte tendenza all’efficacia nella variazione rispetto al basale per ALSFRS-R, SVC e forza. Sulla base dei risultati di FORTITUDE-ALS, COURAGE-ALS (NCT04944784) è stato progettato per testare l’efficacia di reldesemtiv in 555 partecipanti randomizzati (2:1) a ricevere reldesemtiv 300 mg BID o placebo, con un trattamento in doppio cieco per 24 settimane seguito da un periodo di 24 settimane di farmaco attivo in aperto.
COURAGE-ALS è stato interrotto per futilità al momento della seconda analisi ad interim. Reldesemtiv non ha modificato, a 24 settimane, la progressione di ALSFRS-R, della capacità vitale forzata, della forza muscolare o dell’ALS Assessment Questionnare 40 tra soggetti in farmaco e in placebo, indipendentemente dai criteri di inclusione e da diverse stratificazioni cliniche. Sebbene la discordanza tra i risultati dello studio di fase 2 e 3 di Reldesemtiv nella SLA sia sorprendente, COURAGE-ALS non fornisce alcun supporto all’ipotesi che l’attivazione rapida della troponina muscolare scheletrica sia una strategia benefica nella SLA. Lo studio è stato interotto..
<<>>
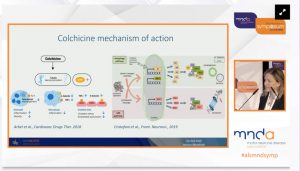 C61: La Prof.ssa Jessica Mandrioli, M.D., PhD dell’Università di Modena e Reggio Emilia, ha presentato i risultati di un trial clinico multicentrico italiano, no profit, condotto in 7 centri italiani con il supporto di AIFA.
C61: La Prof.ssa Jessica Mandrioli, M.D., PhD dell’Università di Modena e Reggio Emilia, ha presentato i risultati di un trial clinico multicentrico italiano, no profit, condotto in 7 centri italiani con il supporto di AIFA.
Il farmaco testato, la colchicina, in studi preclinici era infatti risultato in grado di potenziare l’espressione di fattori legati all’ autofagia (uno dei meccanismi con cui la cellula elimina i prodotti tossici che si accumulano al suo interno) e bloccare l’accumulo di TDP-43, una proteina alterata che rappresenta un segno distintivo della SLA. La colchicina non era mai stata sperimentata prima nei pazienti con SLA.
Lo studio co-ALS, studio multicentrico, randomizzato, in doppio cieco, controllato con placebo, ha incluso pazienti con SLA e insorgenza dei sintomi entro 18 mesi, che sono stati assegnati in un rapporto di 1:1:1 a ricevere colchicina 0,005 mg/kg al giorno, 0,01 mg/kg al giorno o placebo per 30 settimane. L’obiettivo primario era rappresentato dal numero di pazienti che mostravano una diminuzione inferiore a 4 punti nel punteggio totale della Scala di Valutazione Funzionale della SLA-Rivista (ALSFRS-R) dall’inizio alla fine del trattamento, ovvero in 30 settimane. Le misure degli outcomes clinici secondari erano rappresentati dalla misura della progressione della malattia, dalla sopravvivenza, sicurezza e qualità della vita alla fine del trattamento. Gli outcomes biologici secondari erano rappresentati dai cambiamenti dall’inizio alla fine del trattamento negli elementi legati all’autofagia e alla risposta cellulare allo stress, dai cambiamenti dei livelli di TDP-43, dei neurofilamenti e delle vescicole extracellulari, confrontando colchicina e placebo.
Cinquantaquattro pazienti sono stati assegnati al trattamento con colchicina (n=18 per ciascun dosaggio di colchicina) o al placebo (n=18). Il numero di pazienti che mostravano una diminuzione inferiore a 4 punti nel punteggio totale della ALSFRS-R dall’inizio alla fine del trattamento, non differiva significamente tra i gruppi placebo e colchicina: 2 su 15 pazienti (13,3%) nel gruppo placebo; 5 su 15 pazienti (33,3%) nel gruppo colchicina 0,005 mg/kg/giorno (p=0,21) e in 1 su 14 pazienti (7,1%) nel gruppo colchicina 0,01 mg/kg/giorno (p=0,59).
Il farmaco è stato ben tollerato e non si sono verificati più eventi avversi nei trattati rispetto ai soggetti in placebo. Otto pazienti hanno avuto eventi avversi (AE) nel gruppo placebo (44,4%), 3 in colchicina 0,005 mg/kg/giorno (16,7%) e 7 in colchicina 0,01 mg/kg/giorno (35,9%).
Tra le misure biologiche, solo i livelli di TDP43 risultavano più bassi nei trattati con la dose inferiore di farmaco, tuttavia il ridotto numero di campioni esaminati limita notevolmente la riproducibilità del dato. In conclusione, il trattamento con colchicina è risultato sicuro per i pazienti con SLA. L’assenza di risultati statisticamente significativi nella misura di outcome primario, tuttavia, non indica un’efficacia clinica della colchicina in questo contesto. Nonostante qualche debole risultato positivo, per poter pensare di procedere con trials clinici di dimensioni maggiori, sarà necessario comprendere in modo più approfondito se questo farmaco possiede effettivamente un meccanismo d’azione promettente nella SLA.
.
<<>>
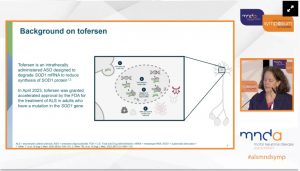 C62: La Dott.ssa Merit Cudkowicz, M.D., MSc., Direttore del Sean M. Healey & AMG Center for ALS presso il Massachusetts General Hospital ha presentato i risultati a due anni dell’estensione in aperto (OLE) dello studio VALOR: Tofersen in adulti con SLA-SOD1. Tofersen è un oligonucleotide antisenso che ha ottenuto dall’FDA l’approvazione accelerata per il trattamento della SLA negli adulti che presentano una mutazione nel gene SOD1 (SOD1-SLA) nell’aprile 2023. L’approvazione è stata supportata dalla riduzione di NfL nel plasma, che sono stati ritenuti ragionevolmente in grado di predire il beneficio clinico nella SOD1-SLA. VALOR è stato uno studio di fase 3, randomizzato, in doppio cieco, controllato con placebo, per valutare gli effetti del tofersen in adulti con SOD1-SLA per 28 settimane. Sebbene l’obiettivo primario (progressione di ALSFRS-R) alla settimana 28 non abbia raggiunto la significatività statistica in VALOR, le tendenze dei marcatori biologici di neurodegeneratizione, associato alle scale di forza e di qualità della vita, supportano un avvio precoce di Tofersen. I partecipanti sono stati randomizzati 2:1 in VALOR a tofersen intratecale (100 mg) o placebo per 6 mesi, dopodiché hanno avuto la possibilità di iscriversi alla fase di estensione dello studio.
C62: La Dott.ssa Merit Cudkowicz, M.D., MSc., Direttore del Sean M. Healey & AMG Center for ALS presso il Massachusetts General Hospital ha presentato i risultati a due anni dell’estensione in aperto (OLE) dello studio VALOR: Tofersen in adulti con SLA-SOD1. Tofersen è un oligonucleotide antisenso che ha ottenuto dall’FDA l’approvazione accelerata per il trattamento della SLA negli adulti che presentano una mutazione nel gene SOD1 (SOD1-SLA) nell’aprile 2023. L’approvazione è stata supportata dalla riduzione di NfL nel plasma, che sono stati ritenuti ragionevolmente in grado di predire il beneficio clinico nella SOD1-SLA. VALOR è stato uno studio di fase 3, randomizzato, in doppio cieco, controllato con placebo, per valutare gli effetti del tofersen in adulti con SOD1-SLA per 28 settimane. Sebbene l’obiettivo primario (progressione di ALSFRS-R) alla settimana 28 non abbia raggiunto la significatività statistica in VALOR, le tendenze dei marcatori biologici di neurodegeneratizione, associato alle scale di forza e di qualità della vita, supportano un avvio precoce di Tofersen. I partecipanti sono stati randomizzati 2:1 in VALOR a tofersen intratecale (100 mg) o placebo per 6 mesi, dopodiché hanno avuto la possibilità di iscriversi alla fase di estensione dello studio.
La somministrazione del Tofersen ha portato a riduzioni del 60-70% dei neurofilamenti nell’arco di 2 anni, indicando un rallentamento sostenuto del danno assonale e della neurodegenerazione, associato ad un rallentamento progressivo degli outcome clinici. Tofersen è stato generalmente ben tollerato con un profilo di sicurezza accettabile. Gli eventi neurologici gravi non sono stati generalmente limitanti per il trattamento e sono stati gestiti con le cure standard.
.
<<>>
 C63: La Dott.ssa Suma Babu, MBBS, MPH del Sean M. Healey & AMG Center for ALS presso il Massachusetts General Hospital ha presentato i risultati di uno studio clinico in doppio cieco, controllato con placebo, di AIT-101 (LAM-002A) nella SLA C9ORF72 – Uno studio clinico di Fase 2a guidato da un biomarcatore e mirato all’inibizione di PIKfyve. PIKfyve è una chinasi che catalizza la fosforilazione in 5 posizioni del fosfatidilinositolo-3-fosfato. L’inibizione attiva il fattore di trascrizione TFEB, che a sua volta regola la clearance autofagosomiale/lisosomiale degli aggregati proteici tossici. AIT-101 (Apilimod dimesilato) è un inibitore di PIKfyve di prima classe, potente e altamente selettivo, che è stato somministrato in modo sicuro a più di 750 soggetti e ha dimostrato efficacia in modelli preclinici di SLA in vitro e in vivo, comprese le mutazioni C9ORF72 e TDP-43. L’obiettivo dello studio era di valutare AIT-101 (LAM-002A) in soggetti affetti da SLA-C9ORF72 in uno studio clinico per verificarne la sicurezza, la tollerabilità, la penetranza nel Sistema Nervoso Centrale e la modulazione di biomarcatori per l’attivazione di TFEB (sGPNMB) e la clearance degli aggregati proteici dipeptidici ripetuti specifici della malattia con mutazione C9ORF72 (Poly(GP)). Gli esiti esplorativi includevano gli effetti sui livelli di NfL e clinici nell’arco di 24 settimane.
C63: La Dott.ssa Suma Babu, MBBS, MPH del Sean M. Healey & AMG Center for ALS presso il Massachusetts General Hospital ha presentato i risultati di uno studio clinico in doppio cieco, controllato con placebo, di AIT-101 (LAM-002A) nella SLA C9ORF72 – Uno studio clinico di Fase 2a guidato da un biomarcatore e mirato all’inibizione di PIKfyve. PIKfyve è una chinasi che catalizza la fosforilazione in 5 posizioni del fosfatidilinositolo-3-fosfato. L’inibizione attiva il fattore di trascrizione TFEB, che a sua volta regola la clearance autofagosomiale/lisosomiale degli aggregati proteici tossici. AIT-101 (Apilimod dimesilato) è un inibitore di PIKfyve di prima classe, potente e altamente selettivo, che è stato somministrato in modo sicuro a più di 750 soggetti e ha dimostrato efficacia in modelli preclinici di SLA in vitro e in vivo, comprese le mutazioni C9ORF72 e TDP-43. L’obiettivo dello studio era di valutare AIT-101 (LAM-002A) in soggetti affetti da SLA-C9ORF72 in uno studio clinico per verificarne la sicurezza, la tollerabilità, la penetranza nel Sistema Nervoso Centrale e la modulazione di biomarcatori per l’attivazione di TFEB (sGPNMB) e la clearance degli aggregati proteici dipeptidici ripetuti specifici della malattia con mutazione C9ORF72 (Poly(GP)). Gli esiti esplorativi includevano gli effetti sui livelli di NfL e clinici nell’arco di 24 settimane.
15 partecipanti con SLA-C9ORF72 sono stati arruolati in uno studio clinico randomizzato, controllato con placebo, della durata di 12 settimane e assegnati a LAM-002A (125 mg/bid) o a placebo in rapporto 2:1, seguito da un OLE di 12 settimane e, successivamente, da un’estensione a lungo termine (in corso) per i partecipanti allo studio (NCT05163886). Gli obiettivi chiave erano le differenze dipendenti dal trattamento nei biomarcatori di sGPNMB nel plasma e nel liquido cerebrospinale (CSF) e nelle proteine poly(GP) dipeptidiche ripetute nel CSF e nelle PBMC dal basale alla settimana 12 nel set di dati dell’analisi dei trattati. Non sono stati osservati eventi avversi gravi o severi correlati al farmaco. Questo studio ha raggiunto gli obiettivi primari e secondari prespecificati della sperimentazione e ha dimostrato la penetrazione nel sistema nervoso centrale. L’AIT-101 ha ridotto drasticamente le ripetizioni dipeptidiche C9ORF72 rilevanti per la malattia nel liquor. E’ stato uno studio clinico precoce guidato da un biomarcatore ben progettato.
Segui gli studi clinici attualmente in corso visitando l’elenco di sperimentazioni SLA-LIVE di conSLAncio.
.
<<>>

C66: “CONNETTIVITÀ STRUTTURALE E FUNZIONALE DEI NETWORK CEREBRALI NEI PAZIENTI AFFETTI DA SLA IN DIVERSI STADI DI MALATTIA”, è stata presentata nella sessione plenaria dal prof. Edoardo Gioele Spinelli.
Di seguito la lista completa degli autori: E.G. Spinelli1-3, A. Ghirelli1,2,5, S. Basaia1, C. Cividini1, N. Riva3,4, T. Russo4,5, E. Canu1, V. Castelnovo1, M. Filippi1-3,5,6, F. Agosta1,2,5
1Neuroimaging Research Unit, Division of Neuroscience, IRCCS San Raffaele Scientific Institute, Milan, Italy;
2Vita-Salute San Raffaele University, Milan, Italy;
3Neurorehabilitation Unit, IRCCS San Raffaele Scientific Institute, Milan, Italy;
4Experimental Neuropathology Unit, Division of Neuroscience, IRCCS San Raffaele Scientific Institute, Milan, Italy;
5Neurology Unit, IRCCS San Raffaele Scientific Institute, Milan, Italy;
6Neurophysiology Service, IRCCS San Raffaele Scientific Institute, Milan, Italy.
Introduzione e Obiettivi: Attualmente non esiste un biomarcatore convalidato per la stadiazione della SLA. L’identificazione di marcatori quantitativi e riproducibili per la stratificazione della malattia è infatti fondamentale per una corretta progettazione e per l’inclusione di coorti di pazienti omogenee negli studi clinici. Il nostro obiettivo è stato quello di valutare le modificazioni della connettività cerebrale strutturale e funzionale sottese agli stadi clinici della SLA, al fine di suggerire misure oggettive e riproducibili fornite dalla connettomica con risonanza magnetica che riflettano la stadiazione della malattia.
Metodi: In questo studio osservazionale, pazienti affetti da SLA e controlli sani sono stati sottoposti a valutazione clinica e RM cerebrale su un dispositivo a 3 Tesla. I pazienti sono stati classificati in 4 gruppi, secondo il sistema di stadiazione del King’s College. Le matrici di connettività cerebrale strutturale e funzionale sono state ottenute utilizzando dati DTI (diffusion tensor imaging) e di RM funzionale a riposo, rispettivamente. Sono state eseguite analisi di statistica network-based (NBS) e sono stati confrontati i valori di connettività intra- e inter-regionale mediante modelli di analisi di covarianza tra i gruppi. Le correlazioni tra misure RM e clinico/cognitive sono state testate utilizzando il coefficiente di Pearson.
Risultati: Sono stati inclusi 104 pazienti con SLA e 61 controlli sani confrontabili per età e sesso. Le analisi NBS e di connettività regionale hanno dimostrato una diminuzione progressiva della connettività strutturale intra- e inter-regionali delle regioni sensorimotorie con l’avanzare delle fasi della SLA, rispetto ai controlli sani. Di contro, la connettività funzionale ha mostrato un andamento divergente tra lo stadio 3 del King’s (aumento di connettività nei circuiti dei gangli della base e temporale [p=0,04 e p=0,05, rispettivamente]) e lo stadio 4 (diminuzione frontotemporale [p=0,03]), suggerendo una complessa interazione tra fenomeni opposti negli stadi più avanzati della malattia. La connettività strutturale intra-regionale sensorimotoria è risultata correlata con il punteggio della Scala di Valutazione Funzionale della SLA – revisionata (ALSFRS-r) (r=0,31, p<0,001) e il carico di segni clinici di compromissione del primo motoneurone (r=-0,25, p=0,01). Anche la connettività strutturale inter-regionale frontale-sensorimotoria è stata correlata con l’ALSFRS-r (r=0,24, p=0,02). Non sono state riscontrate correlazioni con le misure cognitive.
Discussione: La RM cerebrale consente di dimostrare e quantificare una progressiva compromissione della connettività strutturale coinvolgente i network sensorimotori nella SLA, che rispecchia la progressione nei diversi stadi di malattia. Una disconnessione funzionale dei network frontotemporali sembra invece caratterizzare solo le fasi avanzate della malattia. I nostri risultati sostengono l’utilità della connettomica con RM per stratificare i pazienti e per stadiare la patologia cerebrale nella SLA in modo riproducibile, in grado di riflettere la progressione clinica.
.
<<>>
Theme #5: Human Cell Biology
Poster HCB-18: “miRNAs profiling in Peripheral Blood Mononuclear Cells of Fast and Slow progressors Amyotrophic Lateral Sclerosis patients” (Studio dei microRNA per identificare dei marcatori periferici di progressione della malattia nei pazienti affetti da SLA), è stato presentato dalla Dott.ssa Stella Gagliardi, PhD.
Di seguito la lista completa degli autori: F. Dragoni1,2, R. Di Gerlando1,2, M. Garofalo2, L. Diamanti2, B. Rizzo1,2, M. Bordoni2, E. Scarian2, O. Pansarasa2, S. Gagliardi2
¹University of Pavia, Pavia, Italy.
²IRCCS Mondino Foundation, Pavia, Italy.
Razionale: La sclerosi laterale amiotrofica (SLA) è una malattia neurodegenerativa fatale, ad esordio in età adulta, causata dalla perdita selettiva dei motoneuroni superiori e inferiori nella corteccia cerebrale, nel tronco encefalico e nel midollo spinale. Può manifestarsi sporadicamente (sALS), mentre una piccola percentuale di casi di SLA è considerata familiare (fALS). I pazienti, a seconda della progressione della malattia, possono essere classificati come rapidi, intermedi o lenti. Questa classificazione si basa sul valore denominato “Tasso di progressione” (PRL): PRL>1 = Veloce; PRL≥0,5 = Intermedio; PRL<0,5 = Lento.
Il coinvolgimento della regolazione degli RNA nella SLA è stato ampiamente dimostrato. Alcuni studi riguardano il coinvolgimento dei microRNA nella patogenesi della SLA. I miRNA sono piccoli RNA che regolano la traduzione degli RNA codificanti in proteine. I dati emergenti dimostrano che i miRNA sono potenti regolatori dei processi cellulari fisiologici e patologici.
Obiettivi e Metodi: Lo scopo di questo lavoro è identificare, mediante l’approccio Small RNA-Seq, i miRNA alterati nelle cellule mononucleari del sangue periferico (PBMC) di pazienti affetti da sALS, suddivisi in veloci, intermedi e lenti in base alla progressione della malattia e controlli sani per evidenziare nuovi biomarcatori periferici. Ulteriore scopo è identificare i target degli mRNA coinvolti nella progressione della SLA. A questo scopo, abbiamo utilizzato lo strumento bioinformatico “DIANA-TarBase v8”.
Risultati: Non abbiamo trovato alcun miRNA alterato nel gruppo dei pazienti con progressione intermedia. Nel gruppo “rapidi” sono stati segnalati 16 miRNA alterati, mentre nel gruppo “lenti” i miRNA alterati erano 35. Il confronto tra miRNA ha evidenziato 8 miRNA specifici per i pazienti “rapidi” e 27 specifici per quelli “lenti”. Per quanto riguarda i miRNA comuni, 8 di essi sono stati trovati sia nei gruppi “rapidi” che in quelli “lenti”. Il più interessante è risultato il miRNA hsa-miR-183-5p.
Discussione e conclusioni: In conclusione, questo lavoro ci ha permesso di identificare miRNA fenotipo-specifici che possono essere approfonditi come nuovi biomarcatori nella patogenesi della SLA.
.
<<>>
Theme #06: Tissue Biomarkers
Poster BIO-10: “Cross-tissue miRNA analysis of extracellular vesicles and peripheral blood mononuclear cells from ALS patients” (Analisi dei microRNA nelle cellule del sangue periferico e nelle vescicole extracellulari come confronto e interazione tra diversi tessuti), è stato presentato dalla Dott.ssa Stella Gagliardi, PhD.
Di seguito la lista completa degli autori: R. Di Gerlando1,2, F. Dragoni1,2, L. Diamanti2, B. Rizzo2, M. Bordoni2, E. Scarian2, O. Pansarasa2, S. Gagliardi2
¹University of Pavia, Pavia, Italy
²IRCCS Mondino Foundation, Pavia, Italy
³enGenome, 27100 Pavia, Italy
Razionale: L’alterazione dell’espressione genica è considerata un evento chiave nella SLA soprattutto per quanto riguarda i microRNA (miRNA). I miRNA sono molecole che possono essere trasportate attraverso vescicole extracellulari (EV) per agire in combinazione con le proteine fornendo segnali precoci per indicare imminenti cambiamenti neuropatologici nel cervello.
Obiettivi: L’obiettivo è studiare il profilo di espressione dei miRNA nelle EV plasmatiche e fare un confronto con i profili di miRNA ottenuti da cellule mononucleate del sangue periferico (PBMC) per identificare miRNA comunemente espressi e quelli tessuto-specifici.
Metodi: Abbiamo studiato i miRNA contenuti in EV piccole (esosomi, EXO) e grandi (microvescicole, MV) isolati dal plasma di soggetti SLA e soggetti di controllo neurologico mediante sequenziamento di miRNA NGS.
Risultati: Abbiamo confrontato in ciascun tessuto dei pazienti affetti da SLA rispetto ai controlli e abbiamo trovato 159 miRNA alterati in EXO, 247 miRNA in PBMC e 162 miRNA in MV. Successivamente, abbiamo filtrato i miRNA espressi solo in campioni di malattia (non in soggetti sani) per ridurre il numero di miRNA tissutali e specifici per la SLA (EXO n=22, MV=11, PBMC n=8) e abbiamo identificato miRNA tessuto-specifici. I miRNA PBMC-specifici sono stati associati principalmente a pathway neuronali mentre negli EXO abbiamo trovato miRNA implicati nella segnalazione MAPK ed ERB; nelle MV, invece, i pathway alterati non erano specifici.
Discussione: Questo studio mostra il cargo di miRNA differisce significativamente tra le cellule del sangue e la rispettiva frazione di EV. In termini di carico di miRNA, le MV non sono specifiche in relazione alla SLA, quindi gli studi futuri si concentreranno sull’interazione tra cellule ed EXO.
.
<<>>
Poster BIO-11: “Novel insights on the role and therapeutic potential of glycoprotein nonmetastatic melanoma protein B (Gpnmb) in amyotrophic lateral sclerosis” (Nuove analisi sul ruolo e sul potenziale terapeutico della glicoproteina B del melanoma non metastatico (Gpnmb) nella sclerosi laterale amiotrofica), è stato presentato dal Dott. Mauro Giuseppe Spatafora, PhD student.
Di seguito la lista completa degli autori: M.G. Spatafora1, P. Cabras1, G. Di Nolfi1, A. Gazzano1, T. Manilla1, L. Bandirali1, B.M. Custode1, A. Dimartino1, D. Curti1, A. Biffi2, T. Domi3, N. Riva4, A. Quattrini3, M. Peviani1
¹University of Pavia, Pavia, Italy
²University of Padova, Padova, Italy
³San Raffaele Scientific Institute, Milano, Italy
4IRCCS “C. Besta” Neurological Institute, Milano, Italy
Premessa: L’aumento dei livelli di un peptide derivato da Gpnmb nel liquido CSF è stato recentemente associato a una prognosi sfavorevole nei pazienti affetti da sclerosi laterale amiotrofica (SLA). D’altra parte, altri studi hanno evidenziato che l’up-regolazione di Gpnmb potrebbe svolgere un ruolo neuroprotettivo e immunomodulatorio.
Obiettivi: In questo studio, abbiamo intrapreso una caratterizzazione approfondita delle alterazioni di Gpnmb nel modello di ratto transgenico SOD1.G93A (TG) di SLA e nei pazienti, per chiarire il valore di Gpnmb come biomarcatore prognostico e per identificare una finestra temporale precisa, durante il decorso della malattia, adatta per un intervento terapeutico di successo.
Metodi: Abbiamo impiegato l’ibridazione in situ (ISH) e l’immunoistochimica (IHC) nel sistema nervoso centrale e periferico, abbinata alla valutazione dell’ectodominio di Gpnmb (sGpnmb) nel liquor e nel sangue di ratti TG. In parallelo, sGpnmb è stato misurato in una piccola coorte di pazienti affetti da SLA.
Risultati e discussione: Gpnmb è espressa principalmente nei motoneuroni (MN) sani. Tuttavia, negli animali affetti da SLA si assiste a una precoce diminuzione dei livelli di mRNA e della proteina nei MN e a una up-regolazione nella microglia reattiva, dopo l’insorgenza dei sintomi. ISH e IHC hanno evidenziato un ruolo critico delle cellule gliali nella sintesi e nel rilascio di sGpnmb. Parallelamente, abbiamo rilevato un aumento significativo di sGpnmb nel CSF e nel sangue dei ratti TG, così come nei pazienti SLA, quando la patologia è più grave. Dopo aver identificato la dose corretta di Gpnmb per innescare l’attivazione della via neuroprotettiva nel modello di ratto (dimostrata dalla fosforilazione di AKT), stiamo attualmente conducendo un primo studio preclinico atto a verificare il potenziale terapeutico della somministrazione precoce di Gpnmb ricombinante, monitorando parallelamente sGpnmb come biomarcatore per un possibile approccio terapeutico.
.
<<>>
Poster BIO-15: “Increased ADAM 10/17 activity in an animal model of ALS: rationale for targeting ADAMs as a potential therapeutic target?” (Aumentata attività enzimatica di ADAM10/17 in un modello animale di SLA: razionale per considerare ADAM un potenziale target terapeutico?) è stato presentato dal Dott. Paolo Cabras, PhD student.
Di seguito la lista completa degli autori: P. Cabras¹, M.G. Spatafora¹, T. Manilla¹, A. Dimartino¹, A. Demuro¹, F. Invernizzi¹, A. Gazzano¹, M. Peviani¹
¹University of Pavia, Pavia, Italy
Premessa: Le ADAM comprendono una grande famiglia di metalloproteasi responsabili della scissione proteolitica dell’ectodominio (shedding) di proteine transmembrana. ADAM17 è stato originariamente identificato come l’enzima principale per il rilascio di TNF-alfa e l’ADAM10 potrebbe compensare questa funzione. L’attività di ADAM 10/17 è aumentata in condizioni pro-infiammatorie ed è già stata implicata nella patogenesi della malattia di Alzheimer e della sclerosi multipla. Tuttavia, le informazioni sul potenziale coinvolgimento di ADAM10/17 nella SLA sono ancora scarse.
Obiettivi: Il nostro obiettivo è quello di chiarire se le alterazioni dell’espressione, della distribuzione e/o dell’attività enzimatica della proteina ADAM10/17 possano avere un ruolo nella SLA. Inoltre, ADAM10/17 può essere rilasciata in circolo e abbiamo esplorato l’attività di ADAM10/17 nel liquor/sangue come potenziale biomarcatore della SLA.
Metodi: Abbiamo eseguito analisi immunoistochimiche e western blot in distretti del midollo spinale a diversi stadi della malattia nel modello di ratto transgenico SOD1.G93A (TG) di SLA. Parallelamente, abbiamo misurato l’attività di ADAM10/17 negli omogenati di midollo spinale, nel liquor e nel sangue.
Risultati: Abbiamo evidenziato un aumento selettivo dell’immunoreattività di ADAM10/17 nei motoneuroni degli animali TG all’esordio della malattia; con il progredire della malattia verso gli stadi terminali, le ADAM sono up-regolate nelle cellule gliali della sostanza bianca e grigia. L’attività enzimatica di ADAM10/17, misurata negli omogenati di tessuto, è aumentata nella fase sintomatica della malattia. Infine, abbiamo misurato un aumento dei livelli di attività ADAM10/17 solo nel liquor dei TG allo stadio sintomatico, mentre nel sangue era trascurabile.
Discussione: Sebbene i nostri dati siano ancora preliminari, abbiamo evidenziato alterazioni della distribuzione di ADAM10/17 nella fase sintomatica iniziale della malattia. Attualmente stiamo studiando la correlazione tra le ADAM e alcuni dei loro substrati, come il TNF-alfa o il GPNMB, implicati nella malattia; parallelamente, stiamo esplorando inibitori farmacologici selettivi delle ADAM come potenziale approccio terapeutico.
.
.
<<>>
 Poster IMG-26: “Electromechanical coupling study in Amyotrophic Lateral Sclerosis patients as a marker of different progression” (Studio sull’accoppiamento elettromeccanico nei pazienti affetti da Sclerosi Laterale Amiotrofica come possibile marcatore di progressione di malattia), è stato presentato dalla Dott.ssa Laura Libonati, M.D.
Poster IMG-26: “Electromechanical coupling study in Amyotrophic Lateral Sclerosis patients as a marker of different progression” (Studio sull’accoppiamento elettromeccanico nei pazienti affetti da Sclerosi Laterale Amiotrofica come possibile marcatore di progressione di malattia), è stato presentato dalla Dott.ssa Laura Libonati, M.D.
Di seguito la lista completa degli autori: L. Libonati1, C. Cambieri1, M. Ceccanti1, F. Moret1, E. D’Andrea1, G. Tartaglia1, M. Inghilleri1
1Centro Malattie Rare Neuromuscolari Rare, Dipartimento di Neuroscienze Umane, Sapienza
Background: La Sclerosi Laterale Amiotrofica (SLA) è una malattia neurodegenerativa che colpisce i motoneuroni. I pazienti possono essere classificati come slow o fast progressors in base all’indice di progressione (PI). Lo scopo di questo studio è analizzare le differenze tra la forza e l’ampiezza del potenziale d’azione muscolare composto (cMAP) in una coorte di pazienti con ALS.
Materiali e Metodi: Sono stati reclutati 42 pazienti con la SLA, suddivisi in slow o fast progressors. Abbiamo registrato la latenza e l’ampiezza del cMAP dai muscoli flessori delle dita e la forza prodotta dalla stimolazione sovramassimale del nervo mediano al gomito. Abbiamo utilizzato un trasduttore di forza (ZD10-100), fissato su una superficie rigida, sulla quale il paziente appoggiava la mano. Il test è stato eseguito su entrambe le braccia dei pazienti.
Risultati: 22 pazienti erano fast progressors e 22 slow progressors. Non abbiamo riscontrato differenze significative tra latenza (fast 2.54±0.55 ms vs slow 2.43±0.45 ms) e ampiezza (fast 10.45±4.45 mV vs slow 9.49±4.78 mV) del cMAP tra i due gruppi. Abbiamo invece riscontrato una differenza significativa tra l’ampiezza della forza di picco (slow 10.5 ± 5.7 N vs fast 6.3 ± 5.1 N, p=0.005) e l’area sotto la curva (slow 6465 ± 5300 vs fast 3600 ± 3475, p=0,017) registrata tra i due gruppi.
Discussione: La patogenesi della SLA non è ancora chiara, con due ipotesi principali, un modello “dying back” e un modello “dying forward”. Ci sono sempre più prove che il muscolo svolga un ruolo chiave nella patogenesi della SLA. Abbiamo mostrato che pazienti con diverse forme di malattia avevano gli stessi valori di cMAP ma erano in grado di sviluppare forze diverse, con valori più alti negli slow progressors lenti, poiché il muscolo aveva un ruolo diverso in questi pazienti.
Conclusioni: Questo studio ha mostrato come i fast e gli slow progressors sviluppino forze muscolare diverfse a parità di cMAP, suggerendo un possibile ruolo protettivo del muscolo negli slow pazienti progressori lenti.
Riferimenti:
Ceccanti M, et al. Creatine Kinase and Progression Rate in Amyotrophic Lateral Sclerosis. Cells.2020 May 8;9(5):1174.
Nijssen J, Motor neuron vulnerability and resistance in amyotrophic lateral sclerosis. Acta Neuropathol.2017Jun;133(6):863-885
Vogt T, Functional properties of motor units in motor neuron diseases and neuropathies. Electroencephalogr Clin Neurophysiol.1997Aug;105(4):328-32.
.
Il simposio si è concluso con l’assegnazione di due ulteriori premi:

Il Premio Healey Center International Prize for Innovation in ALS 2023. Questo premio di 50.000 dollari è stato conferito al team internazionale che ha stabilito i biomarcatori del neurofilamento NfL come biomarcatore diagnostico e prognostico precoce per la SLA: Prof. Robert Bowser, PhD, Direttore Scientifico, Professore e Direttore del Barrow Neurological Institute (USA); Prof. Martin Turner, MBBS, PhD, FRCP, Professore di Neurologia Clinica e Neuroscienze all’Oxford University (Regno Unito), Prof. Michael Benatar, MBChB, DPhil, Professore di Neurologia all’University of Miami (USA), Prof. Andrea Malaspina, MBBS, PhD, FRCP all’University College London (Regno Unito), Prof. Markus Otto, M.D., Professore all’Universitätsklinikum (Germania), e il team della Biogen Therapeutics, Cambridge, MA (USA). Il Premio Healey Center International Prize for Innovation in ALS viene assegnato ogni anno per riconoscere il lavoro “che porta a scoperte e progressi eccezionali nello sviluppo di terapia per la SLA.”
.
.
.
 Il Drs. Ayeez and Shelena Lalji & Family ALS Endowed Award for Innovative Healing 2023 è stato conferito al gruppo scientifico che ha scoperto lo sviluppo del bersaglio terapeutico (Jacifusen) per le persone affette dalla SLA-FUS: Prof. Neil Shneider, M.D., PhD, Professore Claire Tow dei disturbi del motoneurone alla Columbia University (USA), Prof. Robert Brown, M.D., Dphil, Professore e Direttore di Neuroscienze Donna M. e Robert J. Manning all’University of Massachusetts Memorial Health, Prof.ssa Sandrine De Cruz, Professore, Dipartimento di Neuroscienze al KU Leuven, Dott. Paymaan Jafar-Najad, M.D., Direttore Esecutivo presso Ionis Pharmaceuticals e il Dott. Frank Rigo, PhD, SVP, presso Ionis Pharmaceuticals.
Il Drs. Ayeez and Shelena Lalji & Family ALS Endowed Award for Innovative Healing 2023 è stato conferito al gruppo scientifico che ha scoperto lo sviluppo del bersaglio terapeutico (Jacifusen) per le persone affette dalla SLA-FUS: Prof. Neil Shneider, M.D., PhD, Professore Claire Tow dei disturbi del motoneurone alla Columbia University (USA), Prof. Robert Brown, M.D., Dphil, Professore e Direttore di Neuroscienze Donna M. e Robert J. Manning all’University of Massachusetts Memorial Health, Prof.ssa Sandrine De Cruz, Professore, Dipartimento di Neuroscienze al KU Leuven, Dott. Paymaan Jafar-Najad, M.D., Direttore Esecutivo presso Ionis Pharmaceuticals e il Dott. Frank Rigo, PhD, SVP, presso Ionis Pharmaceuticals.
.
.
.
.
.
.
:
conSLAncio ringrazia, a nome di tutte le persone affette da SLA e tutti gli associati che sostengono la nostra missione.
Il prossimo 35° Simposio Internazionale sulla SLA/MND 2024 avrà luogo presso Montreal, Canada dal 6-8 Dicembre 2024.
Per ulteriori informazioni su conSLAncio, visita: www.conslancio.it
Contatto:
L’ufficio stampa di conSLAncio, scrivere: info@conslancio.it

